CÁC VẤN ĐỀ LIÊN QUAN ĐẾN THUỐC
1.1. Định nghĩa các vấn đề liên quan đến thuốc
Trên thế giới, nhiều định nghĩa về các vấn đề liên quan đến thuốc cùng tồn tại. Các định nghĩa khác nhau phụ thuộc vào mức độ phân loại và mục tiêu của nhà nghiên cứu. Một số thuật ngữ khác như Medical Related Problems, Pharmaceutical Care Issue, Drug Therapy Problem cũng được đề cập trong một số tài liệu. Tuy nhiên, định nghĩa được sử dụng phổ biến nhất hiện nay là định nghĩa theo Hệ thống Chăm sóc Dược Châu Âu (Pharmaceutical Care Network Europe, PCNE) năm 2009: “Một vấn đề liên quan đến thuốc (Drug Related Problems – DRP) là một sự kiện hoặc tình huống liên quan đến điều trị bằng thuốc, mà sự kiện hay tình huống này thực sự hoặc có khả năng can thiệp vào kết quả sức khỏe mong muốn đạt được sau điều trị”. Hai điều kiện phải có đối với một trường hợp được coi là vấn đề liên quan đến thuốc: các triệu chứng phải được quan sát trên một bệnh nhân và những triệu chứng này phải liên quan đến việc sử dụng thuốc.
DRPs bao gồm sai sót trong sử dụng thuốc (Medication error – ME), biến cố bất lợi liên quan đến thuốc (Adverse drug event – ADE) và phản ứng có hại của thuốc (Adverse drug reaction – ADR):
- ME: là bất kỳ biến cố có thể phòng tránh được, có khả năng gây ra hoặc dẫn đến việc sử dụng thuốc không hợp lý, hoặc gây hại cho người bệnh trong khi thuốc được kiểm soát bởi nhân viên y tế, người bệnh, hoặc người sử dụng. Các biến cố như vậy có thể liên quan tới thực hành chuyên môn, các sản phẩm chăm sóc sức khỏe, quy trình và hệ thống bao gồm: kê đơn và quá trình truyền đạt thông tin đơn thuốc; ghi nhãn, đóng gói và danh pháp; pha chế, cấp phát, phân phối; quản lý; giáo dục; giám sát và sử dụng.
- ADE: bất kỳ tổn hại nào do việc sử dụng thuốc gây ra.
- ADR: Theo Luật Dược (2016), phản ứng có hại của thuốc là những phản ứng không mong muốn có hại đến sức khỏe, có thể xuất hiện ở liều dùng bình thường. Theo định nghĩa của Tổ chức Y tế thế giới, phản ứng có hại của thuốc là phản ứng độc hại, không mong muốn và xuất hiện ở liều thường dùng cho người với mục đích phòng bệnh, chẩn đoán, điều trị bệnh hoặc làm thay đổi chức năng sinh lý của cơ thể.
1.2. Các hệ thống phân loại những vấn đề liên quan đến thuốc
Hiện nay có nhiều hệ thống phân loại DRP trên thế giới. Các công cụ phân loại khác nhau giúp mô tả bản chất, tỷ lệ và mức độ phổ biến của DRP, đồng thời tạo cơ sở dữ liệu cho cả nhà nghiên cứu và người thực hành lâm sàng. Trong một số hệ thống phân loại, nguyên nhân của DRP được tách khỏi các vấn đề, trong các hệ thống khác, vấn đề cũng mô tả nguyên nhân. Một số hệ thống phân loại cung cấp thêm nhóm mã hóa cho các biện pháp can thiệp. Tuy nhiên, hệ thống phân loại hiện đại nhất hiện nay bao gồm phân loại theo nhiều cấp độ, trong đó nhóm chính được định nghĩa bao quát và nhóm phụ được phân tích cụ thể hơn. Nhiều cách phân loại có trọng tâm khác nhau, một số tập trung vào quan điểm của bệnh nhân và kết quả của can thiệp, một số khác hướng tới quá trình kê đơn, cấp phát và sử dụng thuốc.
Năm 2002, Schaefer đã mô tả 8 tiêu chí xác định hệ thống mã hóa phù hợp. Với những tiêu chí đó, Van Mil J. F đã xác định 5 yêu cầu chính đối với hệ thống phân loại DRPs như sau:
- Việc phân loại cần có định nghĩa rõ ràng cho nhóm DRP và từng loại DRP.
- Việc phân loại nên được xác định là có giá trị.
- Việc phân loại nên được sử dụng trong thực tế (được dùng trong một nghiên cứu đã công bố).
- Việc phân loại phải có cấu trúc mở, phân cấp (với nhóm chính, nhóm phụ và cấu trúc mở bao gồm vấn đề mới, tốt nhất ở nhóm phụ).
Việc phân loại nên được tập trung vào quá trình và kết quả sử dụng thuốc và tách riêng vấn đề khỏi nguyên nhân.
Hệ thống phân loại PCNE phiên bản 9.1 là hệ thống được sử dụng phổ biến nhất trong các nghiên cứu trên thế giới. Hệ thống này có nhiều ưu điểm như:
- Bao gồm hệ thống phân loại DRP có cấu trúc chi tiết gồm các phần chính, phần phụ, cho phép mã hóa từng loại DRP.
- Một DRP được phân loại theo mức độ ảnh hưởng (ví dụ: hiệu quả điều trị), sau đó theo nguyên nhân (ví dụ: bệnh nhân quên sử dụng thuốc), can thiệp dược và hiệu quả mang lại.
- DRP và từng vấn đề được định nghĩa rõ ràng.
- Công cụ đã được thẩm định thông qua nhiều nghiên cứu khác nhau tại nhà thuốc và bệnh viện trên thế giới và được dịch sang nhiều ngôn ngữ khác nhau.
- Hệ thống phân loại PCNE phiên bản 9.1 (V9.1)
|
Mã V9.1 |
Lĩnh vực cơ bản |
|
| Vấn đề (cũng có thể là tiềm ẩn) | P1 | Hiệu quả điều trị |
| P2 | An toàn | |
| P3 | Khác | |
| Nguyên nhân (bao gồm nguyên nhân có thể và nguyên nhân tiềm ẩn) | C1 | Lựa chọn thuốc |
| C2 | Dạng dùng | |
| C3 | Lựa chọn liều dùng | |
| C4 | Thời gian điều trị | |
| C5 | Cấp phát thuốc | |
| C6 | Quá trình sử dụng thuốc | |
| C7 | Các vấn đề liên quan đến bệnh nhân | |
| C8 | Các vấn đề liên quan đến vận chuyển bệnh | |
| C9 | Khác | |
| Kế hoạch can thiệp | I0 | Không can thiệp |
| I1 | Ở cấp độ người kê đơn | |
| I2 | Ở cấp độ bệnh nhân | |
| I3 | Ở cấp độ thuốc | |
| I4 | Khác | |
| Mức độ đồng thuận của can thiệp | A1 | Chấp nhận can thiệp |
| A2 | Không chấp nhận can thiệp | |
| A3 | Khác | |
| Tình trạng DRP | O0 | Tình trạng vấn đề không được biết |
| O1 | Vấn đề được giải quyết | |
| O2 | Vấn đề được giải quyết 1 phần | |
| O3 | Vấn đề không được giải quyết |
1.3 Cách xác định và đánh giá DRP trong đơn thuốc
Sử dụng một hệ thống phân loại nhất định là nhiệm vụ cơ bản để dược sĩ làm công tác dược lâm sàng xác định, đánh giá và ngăn chặn DRP. Các hệ thống phân loại khác nhau, mỗi dược sĩ lựa chọn bảng phân loại phù hợp với hệ thống cơ sở y tế tại nơi làm việc. Xác định DRP là kiểm tra tính hợp lý về việc sử dụng thuốc bằng cách so sánh chế độ dùng thuốc của bệnh nhân với các hướng dẫn hay khuyến cáo trong nước và trên thế giới. Các nội dung đánh giá sử dụng thuốc bao gồm: lựa chọn thuốc, dạng dùng, liều dùng, thời gian dùng thuốc, cấp phát thuốc, quá trình sử dụng thuốc và các vấn đề khác liên quan đến bệnh nhân.
Theo Hướng dẫn quốc gia về Cảnh giác dược năm 2021, nguồn cơ sở dữ liệu mà dược sĩ có thể tham khảo được thống kê như sau:
Một số nguồn tài liệu tra cứu thông tin chung và chuyên khảo phổ biến tại Việt Nam và trên thế giới.
| Lĩnh vực thông tin | Tên sách/ phần mềm/ công cụ tra cứu |
| Tra cứu thông tin chung | – Dược thư Quốc gia Việt Nam
– Dược thư Quốc gia Việt Nam dùng cho tuyến cơ sở – British National Formulary – AHFS Drug Information – Martindale: The Complete Drug Reference – Drug Information Handbook – Micromedex – Lexicomp |
| Phản ứng có hại của thuốc | – Meyler’s Side Effects of Drugs
– LiverTox (livertox.nih.gov) |
| Tương tác thuốc | – Drug Interactions Micromedex
– Drug Interaction Facts – Stockley’s Drug Interactions (and ompanion handbook) – Hansten and Horn’s Drug Interaction Analysis and Management – Thesaurus des Interactions Médicamenteuses |
| Thuốc có nguồn gốc dược liệu | – Cây thuốc và động vật làm thuốc ở Việt Nam (Viện Dược liệu)
– Natural Medicine Comprehensive Database – Herbal Medicine PDR for Herbal Medicine |
1.4 Các vấn đề liên quan đến thuốc y học cổ truyền
Thuốc dược liệu, thuốc cổ truyền được sử dụng lâu đời trong hệ thống khám bệnh, chữa bệnh và được xem là ít tác dụng không mong muốn. Tuy nhiên, trong thực tế sử dụng, các hiện tượng dị ứng, ngộ độc có liên quan đến dược liệu, thuốc dược liệu và thuốc cổ truyền cũng đã được ghi nhận. Việc sử dụng dược liệu an toàn bao gồm đảm bảo chất lượng dược liệu, thực hành tốt nuôi trồng và sản xuất dược liệu, kiểm nghiệm dược liệu theo các tiêu chuẩn dược điển kết hợp việc sử dụng thuốc dược liệu hợp lý với tình trạng bệnh. Ngoài ra, việc phối hợp thuốc y học cổ truyền phải hết sức tránh các trường hợp tương phản, tương tác,… để tránh các hậu quả khi dùng thuốc cũng như tác dụng kém của thuốc.
Sai sót liên quan đến sử dụng thuốc dược liệu, thuốc cổ truyền có thể xảy ra ở tất cả các giai đoạn, bao gồm: kê đơn thuốc, bào chế, sắc thuốc, cấp phát, hướng dẫn sử dụng, cách dùng thuốc, tuân thủ của bệnh nhân.
Trong quá trình kê đơn:
- Phối ngũ không phù hợp trong quá trình kê đơn: hai vị thuốc tương tác trong cùng một đơn thuốc làm tăng độc tính của thuốc.
- Không ghi rõ cách chế biến vị thuốc cổ truyền làm ảnh hưởng tới tác dụng của thuốc và không đảm bảo an toàn cho người sử dụng. Ví dụ: Chích Hoàng kỳ (Hoàng kỳ chích mật) không dùng cho người bị đái tháo đường mà dùng Sinh Hoàng kỳ (Hoàng kỳ sống); Phụ tử (chưa chế biến) có độc tính cao được chuyển sang dạng Hắc phụ (Phụ tử đã chế biến) sẽ giúp làm giảm độc tính của dược liệu.
- Không ghi rõ hướng dẫn cách sắc thuốc trong đơn thuốc. Ví dụ: không ghi rõ khi sắc Ma hoàng phải hớt bỏ bọt.
- Không ghi rõ thời điểm uống thuốc (lúc đói, lúc no…).
- Không ghi kiêng kỵ khi dùng thuốc. Ví dụ: không ghi rõ khi đang dị ứng thì kiêng thức ăn tanh.
Trong quá trình bào chế:
- Bào chế là một quá trình chế biến dược liệu mang tính đặc thù của Y học cổ truyền nhằm tăng tác dụng của thuốc hoặc giảm bớt độc tính của thuốc. Nếu quá trình bào chế không được thực hiện đúng quy định sẽ không loại trừ được độc tính của thuốc và có thể gây phản ứng có hại khi sử dụng.
- Trong YHCT có nhiều vị thuốc dễ gây ngộ độc, nôn mửa nếu bào chế không kỹ như bán hạ chế, phụ tử chế… Vị thuốc tỳ bà diệp (lá nhót) khi bào chế phải làm sạch các lông tơ trên mặt lá để tránh kích ứng niêm mạc họng, gây ho, sưng niêm mạc.
- Sai sót trong quá trình sắc thuốc, cấp phát, hướng dẫn sử dụng.
- Nhầm lẫn khi sắc thuốc có thể xảy ra nếu không đánh số thang thuốc, phiếu, ấm sắc thuốc, bình đựng thuốc trước khi sắc thuốc; không có tủ giá để sắp xếp phân biệt thuốc chưa sắc, thuốc đang sắc dở, thuốc đã sắc xong; hệ thống sổ sách theo dõi quá trình sắc thuốc và cấp phát thuốc sắc chưa được ghi chép đầy đủ, chưa theo biểu mẫu quy định.
Trong cách dùng thuốc: Nhiều vị thuốc có độc tính cao chỉ được sử dụng bên ngoài như bôi, đắp ngoài da. Ví dụ: mật cá trắm, lá vòi voi dùng đắp ngoài chữa các bệnh lý cơ xương khớp… nếu sử dụng qua đường uống có thể gây suy thận cấp, hoại tử ống thận đe dọa tính mạng người bệnh.
Trong quá trình người bệnh sử dụng thuốc: Việc người bệnh không tuân thủ về cách dùng, thời điểm dùng thuốc theo lời dặn của thầy thuốc, tự ý dùng thuốc dược liệu, thuốc cổ truyền không rõ nguồn gốc hoặc qua truyền miệng có thể là những sai sót dẫn đến xuất hiện phản ứng có hại hoặc độc tính của thuốc dược liệu, thuốc cổ truyền.
Hiện tại có rất ít báo cáo chính thức hay nghiên cứu cụ thể về phản ứng có hại liên quan đến sử dụng dược liệu, thuốc dược liệu và thuốc cổ truyền. Do vậy, việc triển khai các hoạt động Cảnh giác Dược đối với dược liệu, thuốc dược liệu và thuốc cổ truyền cũng như tiến hành các nghiên cứu sâu hơn về dược liệu, thuốc dược liệu và thuốc cổ truyền có nguy cơ gây hại là rất cần thiết
1.5 Sự can thiệp của dược sĩ trên vấn đề liên quan đến thuốc
Có nhiều nội dung can thiệp trên DRP trong đơn thuốc. Một trong những nội dung được sử dụng phổ biến trong các nghiên cứu là theo hệ thống phân loại PCNE, cụ thể như sau:
Tại Việt Nam, năm 2021, ngoài việc ban hành bộ mã DRPs, Bộ Y tế còn quy định các nội dung can thiệp của người làm công tác dược lâm sàng áp dụng cho toàn bộ cơ sở y tế Nhà nước và tư nhân.
|
Vấn đề liên quan đến thuốc |
Can thiệp của người làm công tác DLS |
||||
| Lựa chọn thuốc | T1 | Điều trị chưa đủ | T4 | Thay đổi điều trị | C1 |
| Lặp thuốc | T1.1 | Có bệnh lý chưa được điều trị đủ | T4.1 | Ngừng thuốc | C1.1 |
| Tương tác thuốc | T1.2 | Cần biện pháp dự phòng/ Chưa dự phòng đủ |
T4.2 | Thêm thuốc | C1.2 |
| Sai thuốc* | T1.3 | Vấn đề khác về bệnh lý chưa được điều trị đủ | T4.99 | Tăng/Giảm liều thuốc | C1.3 |
| Đường dùng/ dạng bào chế chưa phù hợp | T1.4 | Độ dài đợt điều trị | T5 | Thay đổi thuốc có hoạt chất khác | C1.4 |
| Có chống chỉ định | T1.5 | Quá ngắn | T5.1 | Thay đổi thuốc có tên thương mại khác có cùng hoạt chất |
C1.5 |
| Không có chỉ định | T1.6 | Quá dài | T5.2 | Thay đổi dạng bào chế | C1.6 |
| Quá nhiều thuốc cho cùng chỉ định | T1.7 | Vấn đề khác về độ dài đợt điều trị | T5.99 | Thay đổi tần suất điều trị | C1.7 |
| Vấn đề khác về lựa chọn thuốc | T1.99 | Cần được theo dõi | T6 | Thay đổi độ dài đợt điều trị | C1.8 |
| Liều dùng | T2 | Biểu hiện lâm sàng | T6.1 | Không có thuốc cung ứng | C1.9 |
| Liều dùng quá cao | T2.1 | Các chỉ số cận lâm sàng | T6.2 | Cần tham khảo thêm | C2 |
| Liều dùng quá thấp | T2.2 | Vấn đề khác cần theo dõi | T6.99 | Hội chẩn can thiệp/ chuyên khoa | C2.1 |
| Tần suất dùng quá nhiều | T2.3 | Độc tính và ADR | T7 | Ý kiến khác trong bệnh viện | C2.2 |
| Tần suất dùng không đủ | T2.4 | Bệnh nhân gặp ADR | T7.1 | Y văn | C2.3 |
| Thời điểm dùng chưa phù hợp | T2.5 | Ngộ độc thuốc | T7.2 | Cung cấp thông tin | C3 |
| Hướng dẫn liều chưa phù hợp, chưa rõ ràng | T2.6 | Cấp phát thuốc | T8 | Tư vấn thêm cho người bệnh | C3.1 |
| Vấn đề khác về liều | T2.99 | Không sẵn có thuốc | T8.1 | Tóm tắt thông tin về thuốc | C3.2 |
| Tuân thủ điều trị của người bệnh | T3 | Không sẵn có hàm lượng | T8.2 | Hỗ trợ tính liều khuyến cáo/ Hướng dẫn sử dụng thuốc | C3.3 |
| Dùng thuốc không đủ liều như được kê đơn | T3.1 | Không sẵn có dạng bào chế | T8.3 | Theo dõi thêm | C4 |
| Dùng thuốc cao hơn liều như được kê đơn | T3.2 | Vấn đề khác về cấp phát thuốc | T8.99 | Giám sát lâm sàng | C4.1 |
| Dùng thuốc không đều như được kê đơn | T3.3 | Vấn đề không được phân loại khác | T99 | Các chỉ số cận lâm sàng | C4.2 |
| Cố ý lạm dụng thuốc | T3.4 | Chú ý cho điều dưỡng | C5 | ||
| Dạng bào chế khó sử dụng | T3.5 | Can thiệp khác | C99 | ||
| Vấn đề khác về tuân thủ của người bệnh | T3.99 | Không có can thiệp | C0 | ||
* Gồm sai tên hoạt chất/tên thuốc/nồng độ/hàm lượng
1.6 Các nghiên cứu khảo sát và can thiệp DRPs
| Tác giả (năm) | Mục tiêu nghiên cứu | Đối tượng nghiên cứu | Thiết kế nghiên cứu | Kết quả nghiên cứu |
| Garin N. (2021) | Khảo sát DRP trên lâm sàng và xác định các nguyên nhân dẫn đến DRP tại bệnh viện. | Bệnh nhân trên 18 tuổi nhập viện tại các khoa Nội, tiêu hóa, lão khoa, thần kinh, hô hấp, tim mạch, ung thư và huyết học tại Bệnh viện ở Bercelona – Tây Ban Nha từ tháng 3/2015 – 02/2016. | Nghiên cứu cắt ngang mô tả. | 1.602 bệnh nhân được đánh giá. Tỷ lệ DRP là 45,1%, đặc biệt cao hơn ở bệnh nhân lớn tuổi, sử dụng nhiều thuốc và đa bệnh lý. DRPs gây ảnh hưởng đến hiệu quả điều trị và tác dụng không mong muốn của thuốc. Nguyên nhân dẫn đến DRPs phổ biến nhất là lựa chọn thuốc và liều lượng thuốc. Can thiệp dược được đồng thuận giúp giảm cải thiện toàn bộ 74,1% DRP và 4,8% DRP cải thiện 1 phần. |
| Belaiche S. (2021) | Đánh giá can thiệp dược lâm sàng thuộc Hiệp hội Dược lâm sàng Pháp trên DRP của bệnh nhân ngoại trú. | Bệnh nhân ngoại trú thuộc dịch vụ y tế gia đình (Home-Based Hospital) từ tháng 05/-2011 – 04/2015 tại Pháp. | Nghiên cứu cắt ngang mô tả. | 20.195 đơn thuốc của 2.878 bệnh nhân đã được phân tích. Nghiên cứu ghi nhận 388 DRP liên quan đến 267 bệnh nhân, liên quan đến tình trạng bệnh chưa được điều trị (24,2%), sử dụng thuốc không có chỉ định (14,7%), sử dụng thuốc không đúng phác đồ điều trị hoặc chống chỉ định (12,6%), giám sát sử dụng thuốc (12,4%). Can thiệp dược được tiến hành trên 186 thuốc, chủ yếu trên nhóm thuốc tạo máu, kháng sinh và thuốc tác động trên hệ tiêu hóa (34%; 16,5% và 14,6%), 87,6% đề xuất của dược sĩ lâm sàng được chấp nhận. |
| FerrándeO.(2019) | Mô tả các vấn đề liên quan đến thuốc ở bệnh nhân nội trú và phân tích mức độ chấp nhận các can thiệp được lâm sàng. | Bệnh nhân nhập viện tại bệnh viện Del Mar – Tây Ban Nha từ ngày 1/1/2014 – 31/12/2015. | Nghiên cứu hồi cứu | 44.870 bệnh nhân được đưa vào nghiên cứu. Có tổng cộng 4.587 vấn đề liên quan đến thuốc được đánh giá. Phổ biến nhất là các lỗi kê đơn liên quan đến việc sử dụng không đúng y lệnh điện tử (18,1%), cần chỉnh liều do suy gan hoặc thận (11,5%). Mức độ chấp nhận can thiệp dược là 81%. Một số biện pháp can thiệp được đồng thuận ở mức độ cao bao gồm: đào tạo về cách sử dụng máy tính, can thiệp y tế trong phẫu thuật, thông tin thuốc, sửa lỗi kê đơn, giao tiếp trực tiếp với bác sĩ kê đơn. |
| Tasaka Y (2018) | Đánh giá hiệu quả can thiệp của dược sĩ bệnh viện DRP tiềm năng. | Thống kê can thiệp dược lâm sàng tại 20 bệnh viện tại tỉnh Ehime Prefecture – Nhật vào khoảng thời gian 04/2015–03/2017. | Nghiên cứu cắt ngang mô tả. | 2.976 can thiệp dược được đưa vào nghiên cứu. 68,2% can thiệp dược cho bệnh nhân trên 65 tuổi. DRP phổ biến nhất là quá liều lượng thuốc, kế đến là thiếu thuốc, chống chỉ định và sử dụng trùng thuốc với cùng tác dụng. Kết quả cho thấy can thiệp dược lâm sàng ngăn ngừa phản ứng không mong muốn của 1.678 thuốc, tiết kiệm được 2.657.820 USD. |
| Bao Z. (2018) | Đánh giá hiệu quả kinh tế và tác động can thiệp dược lâm sàng trên đơn thuốc ngoại trú. | Can thiệp của các dược sĩ trong điều trị ngoại trú tại bệnh viện Đại học Trung Quốc từ ngày 01/01/2011 – 31/12/2016. | Nghiên cứu cắt ngang mô tả. | 101.271 đơn thuốc được đánh giá và can thiệp dược lâm sàng được thực hiện trên 5.155 đơn thuốc. Với sự can thiệp dược, số lượng DRPs giảm từ 1.845 xuống 238, trong khi tỷ lệ DRPs trong toa thuốc giảm từ 12,6% còn 1,22%. Tỷ lệ chi phí/ hiệu quả của hơn thiệp dược > 1 |
| Abunahlah N. (2018) | Tần suất DRP và các yếu tố liên quan đến DRPs. | Bệnh nhân điều trị nội trú tại khoa nội bệnh viện nghiên cứu lớn nhất tại Istanbul – Thổ Nhĩ Kỳ từ ngày 16 – 20/01/2017. | Nghiên cứu cắt ngang mô tả | 100 bệnh nhân được đưa vào nghiên cứu. DRP tiềm năng được tìm thấy ở ít nhất 80% bệnh nhân và 163 DRP tiềm năng được xác định (trung bình 1,6 DRP/ bệnh nhân). Nguyên nhân phổ biến nhất của DRP là sai sót trong lựa chọn thuốc (44,78%), liều dùng (27,61%), và quy trình dùng thuốc (21,47%). Có mối tương quan có ý nghĩa giữa DRPs và tuổi (r=0,4), số lượng thuốc sử dụng (r=0,32), thời gian nằm viện (r=0,25), suy thận (r=-0,34), và tình trạng viêm (r=0,31). Bệnh nhân suy thận, viêm nhiễm, đa bệnh lý và nằm viện kéo dài có nguy cơ cao gặp DRPs hơn. |
| Sayer I. AI-A. (2016) | Khảo sát DRP ở một số cơ sở ngoại trú của một nhóm bệnh viện tại Jordan.
|
Bệnh nhân khám ngoại trú tại khoa tim mạch, nội tiết và hô hấp tại năm bệnh viện lớn ở Jordan từ tháng 9/2012 – 12/2013. | Nghiên cứu cắt ngang mô tả | 2.898 bệnh nhân được đưa vào nghiên cứu (tuổi trung bình: 56,59 ± 13,5 năm). Tổng số DRP được xác định là 32.348, với mức trung bình 11,2 DRP/ bệnh nhân. Các DRP phổ biến là cần bổ sung hoặc tăng cường giám sát sử dụng thuốc, vấn đề tuân thủ và nhận thức của bệnh nhân về hoạt động tự chăm sóc hoặc biện pháp không dùng thuốc. Số lượng DRP lớn có liên quan đến tuổi cao (> 57 tuổi), chưa lập gia đình, trình độ văn hóa từ trung học phổ thông trở xuống, không có bảo hiểm y tế và bệnh nền (tăng huyết áp, đái tháo đường, rối loạn lipid máu, thiếu máu cơ tim, suy tim và bệnh gút). |
| Nguyễn Ánh Nhựt, Nguyễn Hương Thảo (2022) | Đánh giá hiệu quả can thiệp của dược sĩ đối với DRP trên bệnh nhân ngoại trú và các yếu tố nguy cơ của DRP | Đơn thuốc ngoại trú tại 1 bệnh viện tại Cần Thơ từ ngày 01/03/2019 đến 15/03/2019 (giai đoạn trước can thiệp) và 01/08/2019 (giai đoạn sau can thiệp). | Nghiên cứu can thiệp có so sánh trước/sau.
|
Trước can thiệp: 3.352 đơn thuốc được phân tích. Số đơn thuốc có ít nhất 1 DRP là 88,8%. Trong quá trình sau can thiệp, 2.685 đơn thuốc được đánh giá. Số đơn thuốc có ít nhất 1 DRP giảm còn 74,9% (p<0,001). Các can thiệp dươc có hiệu quả trên DRP trong lựa chọn thuốc, liều dùng, tần suất dùng thuốc và thời gian dùng thuốc (p<0,001). Không có sự cải thiện đáng kể của DRP liên quan thời điểm dùng thuốc so với bữa ăn và tương tác thuốc – thuốc. Số lượng DRP tăng lên theo số lượng thuốc kê đơn (kê đơn từ 5 thuốc trở lên) (p<0,001). |
| Lê Trần Thanh Vy, Nguyễn Hương Thảo (2021) | Đánh giá hiệu quả can thiệp của dược sĩ trên các vấn đề liên quan đến thuốc trong đơn thuốc của bệnh nhi ngoại trú tại bệnh viện. | Đơn thuốc ngoại trú của các bệnh nhi có bảo hiểm y tế đến khám tại các phòng khám ngoại trú của bệnh viện Nhi đồng thành phố Cần Thơ từ ngày 02/01/2020 đến 15/01/2020 (giai đoạn trước can thiệp) và từ ngày 25/07/2020 đến 22/08/2020 (giai đoạn sau can thiệp). | Nghiên cứu can thiệp có so sánh trước/sau.
|
Trong 4.218 đơn thuốc trước can thiệp, có 66,1% đơn thuốc có ít nhất một DRP, với trung bình 0,93 ± 0,7 DRPs trên mỗi đơn thuốc.
Sự đồng thuận của các chuyên gia ở mức độ trung bình khi đánh giá sự ảnh hưởng của DRPs: 50,5% đơn thuốc có DRPs làm giảm an toàn; 29,2% làm tăng chi phí; 23,9% làm giảm hiệu quả điều trị. Sau can thiệp, số đơn thuốc có ít nhất một DRP giảm còn 44,5% (p < 0,001). Tỷ lệ từng loại DRPs đều giảm có ý nghĩa sau can thiệp (p < 0,05), trừ DRPs tương tác thuốc. Do đó, tỷ lệ đơn thuốc có DRPs ảnh hưởng đến hiệu quả, an toàn, chi phí đều giảm có ý nghĩa sau can thiệp (p < 0,001). |
Tài liệu tham khảo
- Quyết định 122/QĐ-BYT ngày 11/01/2021 của Bộ trưởng Bộ Y tế về việc ban hành Hướng dẫn Quốc gia về Cảnh giác Dược.
- Quyết định 3547/QĐ-BYT ngày 22/7/2021 của Bộ trưởng Bộ Y tế về việc Ban hành Mẫu phiếu phân tích sử dụng thuốc.
- Bjorkman I.K., Sanner M.A., Bernsten C.B. (2008), “Comparing 4 classifcation systems for drug-related problems: processes and functions”, Res Soc Adm Pharm. 4(4), pp.320–31.
- Nguyen TH, Le VTT et al (2021), Drug-Related Problems in Prescribing for Pediatric Outpatients in Vietnam, Healthcare (Basel). 9(3), 327.
- Grupo de Investigacíon en Aténcion Farmacéutica (2002), “The second Granada consensus on drug-related problems”, Spanish. Ars Pharmaceutica. 43, pp.175–84.
- Allenet B., Bedouch P., Rose F.-X. et al. (2006), “Validation of an instrument for the documentation of clinical pharmacists’ interventions”, Pharm World Sci. 28(4), pp.181–188.
- Mackie C. A. (2002), Randomised controlled trial of medication review. In: Repeat prescribing in general practice: the development and evaluation of methodologies to improve the quality and cost-effectiveness of repeat prescribing (thesis), University of Strathclyde, Glasgow, UK, 2002.
- Crisp G.D., Burkhart J.I., Esserman D.A. et al. (2011), “Development and Testing of a Tool for Assessing and Resolving Medication-Related Problems in Older Adults in an Ambulatory Care Setting: The Individualized Medication Assessment and Planning (iMAP) Tool”, The American Journal of Geriatric Pharmacotherapy. 9(6), pp.451–460.
- Abunahlah N., Elawaisi, A., Velibeyoglu, F. M. & Sancar, M. (2018), “Drug related problems identified by clinical pharmacist at the Internal Medicine Ward in Turkey”, Int. J. Clin. Pharm. 40, pp.360–367.
- Koubaity M., et al. (2019), “Adaptation and validation of PCNE drug-related problem classification v6.2 in French-speaking Belgian community pharmacies”, Int J Clin Pharm. 41(1), pp.244–250.
- Van Mil J. F., Westerlund L.T., Hersberger K.E., Schaefer M.A. (2004), “Drug-Related Problem Classification Systems”, Annals of Pharmacotherapy., 38 (5), pp.859-867.
- Pharmaceutial Care Network Europe Association (2020), PCNE-classification v9.1.
- Kaufmann CP, Stämpfli D, Hersberger KE, et al (2015), “Determination of risk factors for drug-related problems: a multidisciplinary triangulation process”. BMJ Open, 53(3):e006376.
HẠN CHẾ SAI SÓT TRONG SỬ DỤNG THUỐC
2.1 Thực trạng sai sót trong sử dụng thuốc trên thế giới
Sai sót trong sử dụng thuốc (ME) được định nghĩa là “bất kỳ sự kiện nào có thể phòng ngừa được nhưng có thể xảy ra dẫn đến việc sử dụng thuốc không phù hợp và gây hại cho bệnh nhân trong khi thuốc vẫn được chuyên gia chăm sóc sức khỏe, bệnh nhân hoặc người tiêu dùng kiểm soát”.
Hậu quả có hại nghiêm trọng của sai sót về thuốc có thể bao gồm: tử vong, đe dọa tính mạng, nhập viện, khuyết tật, dị tật bẩm sinh.
Bệnh nhân ở các quốc gia có thu nhập thấp và trung bình có nguy cơ gặp phải ME có thể phòng ngừa được cao gấp đôi so với bệnh nhân ở các quốc gia có thu nhập cao.
- WHO ước tính cứ 1 triệu dân thì có 1 người tử vong do ME
- Tại EU với dân số 447 triệu người – 163000 người tử vong do ME mỗi năm
Theo báo cáo của Tổ chức y tế Thế giới (WHO), chi phí liên quan đến ME ước tính khoảng 42 tỷ USD mỗi năm trên toàn cầu (không tính tiền lương bị mất hoặc chi phí chăm sóc sức khoẻ). Một nghiên cứu ở Vương quốc Anh đã tính toán có 237 triệu ME xảy ra trong một năm tại các bệnh viện của nước này. Tại châu Âu, chi phí do ME ước tính lên tới 2 tỷ euro mỗi năm tính trung bình trên từng quốc gia (chiếm 3% tổng chi tiêu y tế quốc gia). Tại Mỹ, Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) nhận được hơn 100.000 báo cáo mỗi năm của Hoa Kỳ liên quan đến nghi ngờ có sai sót về thuốc.
Ở Canada, một số trường hợp sai sót liên quan đến nhầm lẫn giữa hàm lượng nguyên tố và hàm lượng dạng muối của khoáng chất ghi trên nhãn sản phẩm đã được báo cáo. Bộ Y tế Canada đã tiến hành đánh giá các báo cáo sai sót khi sử dụng chế phẩm bổ sung khoáng chất (đặc biệt là các chế phẩm đơn thành phần có canxi, sắt, magie và kẽm) được gửi từ nhân viên y tế. Những sai sót này dẫn đến quá liều, trong một số trường hợp, còn gây thương tổn nghiêm trọng cho bệnh nhân.
Trong một trường hợp cụ thể ở Canada, bệnh nhân được kê đơn sử dụng sản phẩm có nhãn “canxi cacbonat 500 mg” (hình 1). Trong khi chuẩn bị đơn cho bệnh nhân, nhà thuốc đã hiểu sai là mỗi viên sản phẩm này có chứa 500 mg canxi cacbonat trong khi thực tế mỗi viên chứa 500 mg canxi nguyên tố. Hậu quả là bệnh nhân đã dùng liều cao gấp 2,5 lần so với liều được kê đơn, dẫn đến phải nhập viện.
2.2 Nguyên nhân
ME có thể xảy ra do hệ thống thuốc yếu, yếu tố con người như mệt mỏi hoặc điều kiện làm việc kém như khối lượng công việc nặng nề và thiếu nhân viên. Theo ước tính, khối lượng công việc nặng nề và thiếu nhân viên y tế góp phần tới hơn 20% ME. Do đó, nhân viên y tế có liên quan trực tiếp hoặc gián tiếp đến các biến cố bất lợi như vậy, còn được gọi là “nạn nhân thứ hai”, có thể bị tổn hại nghiêm trọng về mặt tinh thần.
Có một số loại ME khác nhau liên quan đến việc kê đơn hoặc sử dụng thuốc, thời gian, giao tiếp, lỗi do con người, cùng những vấn đề khác. EMA đã công bố khoảng từ 0,3% đến 9,1% ME xảy ra khi bắt đầu kê đơn và từ 1,6% đến 2,1% ở khâu phân phối. Thật sự thì, 25% bệnh nhân đái tháo đường týp 2 mắc ít nhất một sai sót về thuốc, phần lớn là do kê đơn sai liều. Ví dụ về các loại ME phổ biến nhất được báo cáo là không đúng liều lượng (34,7%), bỏ liều (40,0%) và sai tốc độ truyền thuốc.
ME có thể xảy ra ở bất kỳ giai đoạn nào trong toàn bộ hệ thống sử dụng thuốc: trong quá trình kê đơn, sao chép (khi nhập thông tin vào hệ thống máy tính), chuẩn bị, phân phối, quản lý và/hoặc theo dõi hoặc khi bệnh nhân uống thuốc. Tỷ lệ sai sót ở một quốc gia theo các giai đoạn sử dụng thuốc đã được báo cáo là: kê đơn (21,3%), sao chép (1,4%), phân phát (15,9%), quản lý (54,4%) và sử dụng thuốc (7,0%).
2.3 Những biện pháp hạn chế sai sót khi kê đơn thuốc
Bằng chứng về ME cho thấy rằng 50–70,2% tác hại đó có thể được ngăn ngừa thông qua các phương pháp tiếp cận có hệ thống toàn diện để đảm bảo an toàn cho bệnh nhân
WHO khuyến nghị ưu tiên ba điều sau để tránh ME và bảo vệ bệnh nhân khỏi tác hại của thuốc:
- Các tình huống có nguy cơ cao: hiểu được các tình huống trong đó có bằng chứng cho thấy rằng có nguy cơ gây hại cao hơn từ một số loại thuốc cụ thể. Các công cụ và công nghệ có thể giúp các chuyên gia chăm sóc sức khỏe sử dụng các loại thuốc có mức cảnh báo cao, đồng thời cũng nâng cao kiến thức và hiểu biết của bệnh nhân về các loại thuốc này.
- Việc tiêu chuẩn hóa các quy trình và thủ tục là rất quan trọng trong trường hợp sử dụng nhiều thuốc. Điều này được áp dụng từ thực hành kê đơn ban đầu đến việc đánh giá thuốc thường xuyên. Công nghệ cũng có thể đóng vai trò hỗ trợ hữu ích bằng cách nâng cao nhận thức và kiến thức của bệnh nhân về quá trình sử dụng thuốc.
- Chuyển tiếp chăm sóc: chuyển đổi chăm sóc (ví dụ như từ nội trú sang ngoại trú) làm tăng khả năng mắc lỗi giao tiếp, có thể dẫn đến ME nghiêm trọng. Giao tiếp tốt là rất quan trọng, bao gồm cả việc so sánh cho bệnh nhân các loại thuốc trước và sau chăm sóc, gọi là đối chiếu thuốc.
FDA tìm cách ngăn ngừa sai sót về thuốc. Trước khi thuốc được chấp thuận đưa ra thị trường, FDA xem xét tên thuốc, nhãn mác, bao bì và thiết kế sản phẩm để xác định và sửa đổi thông tin có thể góp phần gây ra sai sót về thuốc. Ví dụ: FDA đánh giá:
- Đề xuất tên độc quyền (nhãn hiệu) để giảm thiểu nhầm lẫn giữa các tên thuốc. Với sự trợ giúp của các đơn thuốc mô phỏng và các mô hình trên máy tính, FDA xác định khả năng chấp nhận các tên độc quyền được đề xuất để giảm thiểu các sai sót về thuốc liên quan đến nhầm lẫn tên sản phẩm.
- Nhãn bao bì giúp các nhà cung cấp dịch vụ chăm sóc sức khỏe và người tiêu dùng lựa chọn sản phẩm thuốc phù hợp. Nếu một loại thuốc được sản xuất với nhiều hàm lượng – ví dụ: 5 mg, 10 mg và 25 mg – nhãn của ba loại hộp đựng đó phải dễ phân biệt. Thiết kế nhãn có thể sử dụng các màu sắc khác nhau hoặc xác định cường độ bằng số và chữ in đậm lớn.
- Thông tin kê đơn và bệnh nhân nhằm đảm bảo hướng dẫn kê đơn, pha chế và sử dụng rõ ràng, dễ đọc.
- Sau khi thuốc được phê duyệt và lưu hành tại Hoa Kỳ, FDA sẽ theo dõi và đánh giá các báo cáo ME. FDA có thể yêu cầu nhà sản xuất sửa lại nhãn, ghi nhãn, bao bì, thiết kế sản phẩm hoặc tên độc quyền để ngăn ngừa ME. FDA cũng có thể phát hành các thông tin cảnh báo công chúng về vấn đề an toàn do sai sót thuốc, thông qua Truyền thông An toàn Thuốc, Cảnh báo An toàn Thuốc, Hướng dẫn Thuốc và Podcast về An toàn Thuốc.
- FDA hợp tác với các bên liên quan bên ngoài, cơ quan quản lý, tổ chức an toàn bệnh nhân như Viện Thực hành Thuốc An toàn (ISMP), các tổ chức thiết lập tiêu chuẩn như Dược điển Hoa Kỳ và các nhà nghiên cứu để hiểu nguyên nhân gây ra sai sót về thuốc, hiệu quả của các biện pháp can thiệp nhằm ngăn ngừa chúng và để giải quyết các vấn đề an toàn rộng hơn có thể góp phần gây ra sai sót về thuốc.
- Để củng cố việc đưa đúng thuốc đến đúng bệnh nhân FDA cũng đưa ra các quy định yêu cầu mã vạch trên một số nhãn thuốc và sản phẩm sinh học. Mã vạch cho phép các chuyên gia chăm sóc sức khỏe sử dụng thiết bị quét mã vạch để xác minh rằng đúng loại thuốc – đúng liều lượng và đúng đường dùng – đang được cung cấp cho đúng bệnh nhân vào đúng thời điểm. Hệ thống này nhằm giúp giảm số lượng sai sót về thuốc xảy ra ở bệnh viện và các cơ sở chăm sóc sức khỏe khác.
- FDA đã xuất bản một số hướng dẫn nhằm giúp các nhà sản xuất thiết kế nhãn thuốc, dán nhãn, đóng gói và chọn tên thuốc theo cách giảm thiểu hoặc loại bỏ các nguy cơ có thể góp phần gây ra sai sót về thuốc. Ví dụ: vào năm 2016, FDA đã ban hành hướng dẫn cuối cùng có tiêu đề Những cân nhắc về an toàn khi thiết kế sản phẩm để giảm thiểu sai sót về thuốc.
Năm 2006, FDA đã sửa đổi các quy định về nội dung và hình thức thông tin kê đơn đối với thuốc kê đơn và các sản phẩm sinh học. Giao diện mới giúp các chuyên gia chăm sóc sức khỏe tìm thấy thông tin họ cần dễ dàng và nhanh chóng hơn.
Người tiêu dùng đóng vai trò quan trọng:
Người tiêu dùng cũng có thể đóng một vai trò quan trọng trong việc giảm sai sót về thuốc. Dưới đây là một số lời khuyên về an toàn thuốc:
- Biết các rủi ro khác nhau và nguyên nhân gây ra sai sót trong dùng thuốc.
- Xem trang web dành cho người tiêu dùng của ISMP, ConsumerMedSafety.org, để biết các công cụ và tài nguyên hữu ích nhằm bảo vệ bạn khỏi các sai sót về thuốc.
- Tìm hiểu loại thuốc bạn đang dùng và tác dụng của nó. Thay vì chỉ để bác sĩ viết đơn thuốc và gửi cho bạn trên đường đi, hãy nhớ hỏi tên thuốc và mục đích của thuốc.
- Tìm hiểu cách dùng thuốc và đảm bảo bạn hiểu hướng dẫn. Hỏi xem thuốc có cần được giữ trong tủ lạnh không.
- Kiểm tra nhãn hộp mỗi lần bạn dùng thuốc. Điều này đặc biệt quan trọng nếu bạn đang dùng nhiều loại thuốc vì nó sẽ làm giảm nguy cơ vô tình uống nhầm thuốc.
- Giữ thuốc được lưu trữ trong hộp đựng ban đầu của chúng. Nhiều viên thuốc trông giống nhau, vì vậy việc giữ chúng trong hộp đựng ban đầu sẽ giúp bạn biết tên thuốc và cách dùng. Nếu bạn gặp khó khăn trong việc sử dụng nhiều loại thuốc, hãy hỏi bác sĩ hoặc dược sĩ về những trợ giúp hữu ích.
- Giữ một danh sách cập nhật tất cả các loại thuốc được sử dụng vì lý do sức khỏe, bao gồm thuốc OTC, thuốc bổ sung, dược liệu và các chất khác. Đưa một bản sao của danh sách này cho nhà cung cấp dịch vụ chăm sóc sức khỏe của bạn.
- Nhận thức được nguy cơ tương tác thuốc/thuốc hoặc thuốc/thực phẩm.
- Nếu nghi ngờ hoặc bạn có thắc mắc về thuốc của mình, hãy hỏi dược sĩ hoặc nhà cung cấp dịch vụ chăm sóc sức khỏe khác.
- Báo cáo các nghi ngờ về ME cho cán bộ y tế.
Tài liệu tham khảo
- http://canhgiacduoc.org.vn/CanhGiacDuoc/DiemTin/2425/Bo-Y-te-Canada-sai-sot-lien-quan-mot-so-che-pham-bo-sung-khoang-chat.htm
- Elliott RA, Camacho E, Jancovic D, Sculpher MJ, Faria R, Economic analysis of the prevalence and clinical and economic burden of medication error in England. BMJ Qual Saf, 2021; 30:96–105
- The urgent need to reduce medication errors in hospitals to prevent patient and second victim harm [White paper], European Collaborative Action On Medication Errors and Traceability (ECAMET); 2022
- Mader JK, Aberer F, Drechsler KH, Pottler T, Lichtenegger KM, Kole W et al. Medication errors in type 2 diabetes from pateints’ perspective. PLoS One. 2022;17(4):e0267570.
- Delgado MCM, Alvarez JT, Lopez ES, Gomez MR, Galindo AS, Moro MN et al, Medication error prevention in adult, paediatric and neonate intensive care units in Spain. Madrid: PREVEMED
- Medication without harm: global patient safety challenge on medication safety. Geneva: WHO; 2017.
- https://www.fda.gov/drugs/information-consumers-and-patients-drugs/working-reduce-medication-errors
- https://www.ema.europa.eu/en/news/tackling-medication-errors-european-medicines-agency-workshop-calls-coordinated-eu-approach#:~:text=About%20medication%20errors&text=In%20Europe%2C%20the%20medication%2Derror,between%201.6%20and%202.1%25%20respectively.
NGUY CƠ NHIỄM ĐỘC THẦN KINH KHI SỬ DỤNG CEPHALOSPORIN
Các báo cáo về nhiễm độc thần kinh khi sử dụng kháng sinh cephalosporin bao gồm rối loạn chức năng não bộ (encephalopathy), cơn động kinh và/hoặc động kinh rung giật cơ đã được ghi nhận.
Các yếu tố nguy cơ xuất hiện các phản ứng này bao gồm: nhóm bệnh nhân cao tuổi, suy giảm chức năng thận, có bệnh lý nền về rối loạn thần kinh trung ương và sử dụng cephalosporin đường tiêm tĩnh mạch.
Cân nhắc sử dụng cephalosporin do tiềm ẩn nguy cơ gây nhiễm độc thần kinh ở những người có các yếu tố nguy cơ trên và có tình trạng bệnh thần kinh mới khởi phát không rõ nguyên nhân.
3.1 Nhiễm độc thần kinh có thể xuất hiện khi sử dụng bất kỳ cephalosporin thế hệ nào
Cephalosporin là kháng sinh beta-lactam phổ rộng, thuốc có thể được sử dụng trong phác đồ điều trị đầu tay (first-line) và phác đồ điều trị thay thế (second-line) trong nhiều bệnh lý nhiễm khuẩn.
Cephalosporins bao gồm 5 thế hệ, dựa trên đặc tính phổ kháng khuẩn và lịch sử nghiên cứu phát triển thuốc.
Bảng 1: Phân loại kháng sinh cephalosporins theo thế hệ lưu hành tại New Zealand
| Thế hệ 1 | Thế hệ 2 | Thế hệ 3 | Thế hệ 4 | Thế hệ 5 |
| Cefazolin | Cefuroxim | Cefotaxim | Cefepim | Ceftarolin fosamil |
| Cefalexin | Cefaclor | Ceftazidim | Ceftolozan* | |
| Ceftriaxon |
* Ceftolozan ở dạng phối hợp với tazobactam
Các báo cáo ca và báo cáo chuỗi trên thế giới cho thấy, so với các kháng sinh cephalosporin khác, nhiễm độc thần kinh chủ yếu ghi nhận được khi sử dụng cefepime. Tuy nhiên phản ứng này cũng đã được báo cáo đối với các kháng sinh cephalosporin thế hệ khác.
3.2 Nhiễm độc thần kinh gây ra bởi cephalosporin có thể biểu hiện bằng nhiều các phản ứng khác nhau
Các báo cáo về nhiễm độc thần kinh do cephalosporin được mô tả chủ yếu với các tình trạng rối loạn chức năng liên quan đến bệnh lý não, cơn động kinh và động kinh rung giật cơ.
Bệnh lý não (encephalopathy) là thuật ngữ rộng bao hàm tất cả các bệnh lý làm rối loạn chức năng não bộ, như thay đổi trạng thái tinh thần, biểu hiện thông qua một loạt các triệu chứng từ lú lẫn đến suy giảm ý thức.
Các cơn động kinh liên quan đến dùng cephalosporin có thể biểu hiện dưới dạng co giật hoặc không co giật với cơ chế cephalosporin làm rối loạn chức năng của chất dẫn truyền thần kinh gamma-aminobutyric acid (GABA).
Các triệu chứng nhiễm độc thần kinh được báo cáo xuất hiện trong vòng vài ngày từ lúc bắt đầu điều trị và biến mất sau khi ngừng thuốc.
3.3 Suy giảm chức năng thận là một yếu tố nguy cơ, đặc biệt nếu bệnh nhân không được hiệu chỉnh liều
Cephalosporin được thải trừ qua thận. Ở những bệnh nhân suy giảm chức năng thận có thể gặp tình trạng tích lũy cephalosporin, nếu không hiệu chỉnh liều phù hợp có thể dẫn đến nguy cơ gặp độc tính.
Các yếu tố nguy cơ khác đối với nhiễm độc thần kinh khi sử dụng cephalosporin như: bệnh nhân cao tuổi, rối loạn thần kinh trung ương và sử dụng cephalosporin đường tiêm tĩnh mạch với liều cao.
Những bệnh nhân có tình trạng bệnh lý nền nặng có thể tăng nhạy cảm với các phản ứng nhiễm độc thần kinh do tăng khả năng xâm nhập của cephalosporin vào thần kinh trung ương.
3.4 Lời khuyên cho nhân viên y tế
Nhận biết về nhiễm độc thần kinh khi sử dụng cephalosporin cho bệnh nhân là một thách thức lớn bởi bệnh nhân dùng kháng sinh thường đi kèm với nhiều yếu tố nguy cơ tiềm ẩn.
Tháng 12 năm 2022, MARC đã khuyến cáo các nhân viên y tế nên cân nhắc nguy cơ xảy ra tình trạng nhiễm độc thần kinh khi sử dụng cephalosporin ở những bệnh nhân có các yếu tố nguy cơ nêu trên và tình trạng bệnh lý thần kinh mới khởi phát không rõ nguyên nhân. Trong những trường hợp như vậy, việc ngừng thuốc có thể là phù hợp.
3.5 Các báo cáo ca ở New Zealand
Kể từ ngày 31 tháng 10 năm 2022, Trung tâm theo dõi phản ứng có hại của thuốc tại New Zealand (CARM) đã nhận được một số báo cáo mô tả tình trạng nhiễm độc thần kinh gây ra khi sử dụng cephalosporin (Bảng 2).
Các phản ứng bất lợi được báo cáo trong những trường hợp này bao gồm cơn động kinh, cơn co giật cơ, lú lẫn, bệnh lý rối loạn chức năng não bộ, kích động, ảo giác và mê sảng
Bảng 2: Các trường hợp có khả năng nhiễm độc thần kinh do cephalosporin gây ra được báo cáo về Trung tâm theo dõi phản ứng có hại của thuốc tại New Zealand (CARM), kể từ ngày 31 tháng 10 năm 2022
| Thế hệ | Cephalosporin | Số báo cáo | CARM IDs |
| 1 | Cefazolin | 7 | 58339, 77512, 86695, 97392, 105241, 122558, 137985 |
| Cefalexin | 2 | 123136, 136282 | |
| 2 | Cefuroxim | 6 | 24559, 26025, 26764, 52754, 57256, 87469 |
| Cefaclor | 3 | 22512, 33509, 50548 | |
| 3 | Cefotaxim | 2 | 26764, 105295 |
| Ceftazidim | 2 | 28172, 136000 | |
| Ceftriaxon | 2 | 107950, 110187 | |
| 4 | Cefepim | 2 | 98398, 108616 |
Chú ý:
+ Không có báo cáo của cephalosporin thế hệ 5: ceftarolin và ceftolozan
+ Báo cáo 26764 có 2 thuốc nghi ngờ là cefuroxim và cefotaxim
Tài liệu tham khảo
- Best Practice Advocacy Centre (bpacNZ), 2011, Appropriate use of Cephalosporins, Best Practice Journal41: 22–8.
- Bui T and Preuss CV, 2022, Cephalosporins, In: StatPearls [Internet] 6 November 2022.
- Lacroix C, Kheloufi F, Montastruc F, et al. 2019, Serious central nervous system side effects of cephalosporins: A national analysis of serious reports registered in the French Pharmacovigilance Database, Journal of the Neurological Sciences 398: 196–201.
- Bhattacharyya S, Darby RR, Raibagkar P, et al. 2016, Antibiotic-associated encephalopathy, Neurology86(10):963–71.
- Triplett JD, Lawn ND, Chan J, et al. 2019, Cephalosporin-related neurotoxicity: Metabolic encephalopathy or non-convulsive status epilepticus? Journal of Clinical Neuroscience 67: 163–6.
- Chalela J. 2022, Acute toxic-metabolic encephalopathy in adults.
- 2022, Minutes of the 192nd Medicines Adverse Reaction Committee meeting, 23 December 2022
DỰ PHÒNG NGUY CƠ NHIỄM TOAN LACTIC KHI SỬ DỤNG METFORMIN
Khuyến cáo dành cho nhân viên y tế và bệnh nhân về nguy cơ nhiễm toan lactic khi sử dụng metformin, đặc biệt ở những bệnh nhân suy giảm chức năng thận, mắc bệnh về tim mạch hoặc sepsis (nhiễm khuẩn nghiêm trọng).
Nhiễm toan lactic là phản ứng có hại của metformin và có thể dẫn đến tử vong nếu không xử trí kịp thời. Bệnh nhân có nguy cơ nhiễm toan lactic và có các dấu hiệu của nhiễm toan lactic cần được tư vấn y tế khẩn cấp.
Metformin là thuốc đào thải qua thận, được chỉ định để điều trị đái tháo đường tuýp 2. Nguy cơ nhiễm toan lactic khi sử dụng metformin tăng lên đối với các bệnh nhân suy giảm chức năng thận. Dưới đây là một số biện pháp nhằm hạn chế nguy cơ nhiễm toan lactic:
– Theo dõi chức năng thận và chỉ định liều metformin phù hợp với chức năng thận.
– Đánh giá nguy cơ suy giảm chức năng thận: sử dụng các thuốc gây độc thận và/hoặc khả năng mất nước có thể làm tăng nguy cơ nhiễm toan lactic.
– Ngừng sử dựng metformin và tăng cường theo dõi chức năng thận trong trường hợp tiêm thuốc cản quang chứa iod, lưu ý cần đảm bảo cơ thể người bệnh đủ nước.
– Ngừng sử dụng metformin tạm thời khi có tình trạng mất nước cấp tính (do tiêu chảy, nôn mửa dữ dội, sốt hoặc do giảm lượng nước uống vào) và tái sử dụng thuốc khi lượng nước trong cơ thể trở về mức bình thường đồng thời không có tình trạng suy giảm chức năng thận.
– Thận trọng đối với bệnh nhân đái tháo đường không kiểm soát và/hoặc có tình trạng cấp tính và/hoặc có bệnh mạn tính ở trạng thái mất bù (nhồi máu cơ tim gần đây, suy tim cấp, suy hô hấp, sốc) có khả năng làm thay đổi chức năng thận, dẫn đến nguy cơ nhiễm toan lactic.
Khuyến cáo dự phòng nguy cơ nhiễm toan lactic khi sử dụng metformin
– Các triệu chứng lâm sàng gợi ý tình trạng nhiễm toan lactic ở bệnh nhân:
+ Nôn nhiều lần
+ Đau bụng
+ Chuột rút và đau cơ lan tỏa
+ Cảm giác khó chịu và mệt mỏi nhiều
+ Khó thở
+ Hạ thân nhiệt và giảm nhịp tim.
– Chỉ định chế độ liều theo hướng dẫn trong tờ tóm tắt các đặc tính sản phẩm phù hợp với chức năng thận của bệnh nhân và thường xuyên theo dõi chức năng thận bằng cách tính toán độ thanh thải creatinin.
– Chống chỉ định với các trường hợp:
+ Có bất kỳ tình trạng nhiễm toan chuyển hóa cấp tính nào (nhiễm toan lactic, nhiễm toan ceton)
+ Suy thận nặng (độ thanh thải creatinin <30 mL/phút)
+ Tiền hôn mê do đái tháo đường;
+ Các tình trạng cấp tính có khả năng làm thay đổi chức năng thận như: mất nước, nhiễm trùng nặng, sốc;
+ Mắc bệnh cấp tính hoặc bệnh mạn tính có tình trạng mất bù của như: nhồi máu cơ tim gần đây, suy tim mất bù, suy hô hấp, sốc;
+ Suy tế bào gan, ngộ độc rượu cấp tính, nghiện rượu.
– Lưu ý về nguy cơ xảy ra tương tác thuốc, bao gồm:
+ Không khuyến cáo sử dụng đồng thời metformin với các thuốc cản quang có chứa iod do có thể gây suy giảm chức năng thận thoáng qua hoặc làm nặng thêm tình trạng suy thận đã có từ trước: dừng sử dụng metformin trước hoặc tại thời điểm chẩn đoán hình ảnh. Chỉ tái sử dụng thuốc sau tối thiểu 48 giờ, với điều kiện chức năng thận ổn định sau khi đánh giá lại. Trước và sau khi chụp, cần bù nhiều nước (uống ít nhất 2 lít nước), có thể tiêm tĩnh mạch trong trường hợp giảm thể tích tuần hoàn (đái tháo đường kiểm soát kém hoặc glucose niệu do thuốc lợi tiểu thẩm thấu).
+ Một số thuốc có khả năng làm thay đổi chức năng thận: thuốc hạ huyết áp (thuốc ức chế men chuyển, thuốc đối kháng thụ thể angiotensin II), thuốc lợi tiểu, thuốc kháng viêm không steroid (NSAID), kháng sinh nhóm sulfonamid và aminosid. Khi các thuốc này được sử dụng đồng thời với metformin, nồng độ metformin trong huyết tương có thể tăng lên và có thể cần phải hiệu chỉnh liều metformin để giảm nguy cơ nhiễm toan lactic.
– Cần thông báo cho bệnh nhân về:
+ Nguy cơ nhiễm toan lactic có thể xảy ra khi sử dụng metformin
+ Các tình trạng có thể dẫn đến nhiễm toan lactic như nhiễm trùng nặng, mất nước, bệnh đái tháo đường kiểm soát kém hoặc rối loạn tiêu hóa (tiêu chảy, nôn mửa)
+ Cần duy trì uống đủ nước, đặc biệt là trong giai đoạn nhiễm trùng, rối loạn tiêu hóa hoặc trước khi thực hiện chẩn đoán hình ảnh có tiêm thuốc cản quang chứa iod.
+ Các triệu chứng của nhiễm toan lactic cần được tư vấn y tế kịp thời.
– Nên tạm thời dừng điều trị bằng metformin:
+ Tại thời điểm sử dụng thuốc cản quang có chứa iod theo khuyến cáo của tờ thông tin sản phẩm
+ Trong trường hợp bệnh nhân bị mất nước (do tiêu chảy, nôn mửa, sốt hoặc do giảm lượng nước uống vào), nên tạm thời ngừng sử dụng metformin và cần liên hệ ngay với nhân viên y tế.
+ Trong trường hợp có các triệu chứng lâm sàng gợi ý nhiễm toan lactic: tạm thời ngừng sử dụng metformin (trong khi chờ tư vấn y tế) là an toàn, do nguy cơ nhiễm toan lactic có thể gây tử vong.
Tài liệu tham khảo
https://ansm.sante.fr/actualites/acidose-lactique-et-metformine-un-risque-evitable
NGUY CƠ XẢY RA PHẢN ỨNG CÓ HẠI NGHIÊM TRỌNG LIÊN QUAN ĐẾN KHÁNG SINH FLUOROQUINOLON
Thuốc Fluoroquinolone là nhóm kháng sinh phổ rộng có tác dụng tiêu diệt vi khuẩn và chống nhiễm trùng. Chúng được sử dụng để điều trị một số loại bệnh nhiễm trùng nghiêm trọng khi các loại kháng sinh khác không phù hợp.
5.1 Khuyến cáo của Cơ quan Quản lý Dược phẩm Anh (MHRA)
Cơ quan Quản lý Dược phẩm Anh (MHRA) nhắc lại cảnh báo về nguy cơ xuất hiện phản ứng có hại kéo dài hoặc gây tàn tật không hồi phục liên quan đến kháng sinh fluoroquinolon (ciprofloxacin, delafloxacin, levofloxacin, moxifloxacin, ofloxacin). MHRA khuyến cáo không kê đơn fluoroquinolon trong trường hợp nhiễm khuẩn ở mức độ nhẹ tới trung bình (như đợt cấp của viêm phế quản mạn tính và bệnh phổi tắc nghẽn mạn tính), nhiễm khuẩn không nghiêm trọng hoặc có thể tự khỏi mà không cần điều trị, trừ khi không có kháng sinh phù hợp thay thế. MHRA khuyến cáo ngừng điều trị bằng fluoroquinolon khi bắt đầu xuất hiện dấu hiệu của phản ứng có hại, bao gồm đau hoặc viêm gân.
Fluoroquinolon dùng đường toàn thân và đường khí dung có nguy cơ gây ra phản ứng có hại nghiêm trọng, gây tàn tật kéo dài và không hồi phục. Những phản ứng này được ghi nhận trên các bệnh nhân trong mọi độ tuổi với bất kể các yếu tố nguy cơ kèm theo, và có thể ảnh hưởng khác nhau trên các hệ cơ quan, bao gồm hệ cơ xương, thần kinh, tâm thần và giác quan. Một trong số đó là tổn thương gân (thông thường trên gân Achilles nhưng các gân khác có thể bị ảnh hưởng) xảy ra trong vòng 48 giờ kể từ khi bắt đầu dùng thuốc, hoặc có thể xuất hiện muộn sau vài tháng và biểu hiện rõ rệt sau khi ngừng thuốc.
Hiện nay, chưa có thuốc nào điều trị hiệu quả các những tác dụng không mong muốn được đề cập ở trên. Tuy nhiên, MHRA khuyến cáo cần đánh giá chính xác các triệu chứng này và dừng điều trị bằng fluoroquinolon ngay khi bắt đầu xuất hiện các dấu hiệu của phản ứng có hại.
Giới hạn chỉ định fluoroquinolon được ban hành năm 2019 nhằm giảm thiểu nguy cơ xuất hiện phản ứng có hại kể trên. Không nên kê đơn fluoroquinolon trong điều trị nhiễm khuẩn ở mức độ nhẹ đến trung bình (như đợt cấp của viêm phế quản mạn tính và bệnh phổi tắc nghẽn mạn tính), trừ khi không có không có kháng sinh phù hợp thay thế, bao gồm:
– Đề kháng với những kháng sinh lựa chọn đầu tay thường được khuyến cáo.
– Chống chỉ định với kháng sinh lựa chọn đầu tay thường được khuyến cáo.
– Ghi nhận các tác dụng không mong muốn và không thể tiếp tục điều trị với kháng sinh lựa chọn đầu tay được khuyến cáo.
– Thất bại điều trị với những kháng sinh lựa chọn đầu tay khác.
5.2 Khuyến cáo của Cơ quan Dược phẩm châu Âu (EMA)
Ủy ban an toàn của EMA (PRAC) đang nhắc nhở các chuyên gia chăm sóc sức khỏe rằng việc sử dụng kháng sinh fluoroquinolone qua đường uống, tiêm hoặc hít bị hạn chế do nguy cơ gây tàn tật, tác dụng phụ kéo dài và có khả năng không hồi phục liên quan đến hệ thần kinh, gân, cơ và khớp.
Những hạn chế này được đưa ra vào năm 2019 sau cuộc đánh giá trên toàn EU về những tác dụng phụ rất hiếm gặp nhưng nghiêm trọng này. Một nghiên cứu do EMA tài trợ đã chỉ ra rằng mặc dù việc sử dụng kháng sinh fluoroquinolone đã giảm nhưng những loại thuốc này vẫn có thể được kê đơn ngoài mục đích sử dụng được khuyến nghị.
Chuyên gia chăm sóc sức khỏe (DHPC) nhấn mạnh rằng những kháng sinh fluoroquinolone chỉ nên được kê đơn cho những chỉ định đã được phê duyệt và sau khi đánh giá cẩn thận về lợi ích và rủi ro ở từng bệnh nhân.
5.3 Thông tin cho nhân viên y tế
Khuyến cáo bệnh nhân ngừng sử dụng thuốc và liên hệ với nhân viên y tế nếu ghi nhận xuất hiện các dấu hiệu của phản ứng có hại nghiêm trọng bao gồm viêm gân hoặc đứt gân, đau cơ, yếu cơ, đau khớp, sưng khớp hoặc những ảnh hưởng trên thần kinh ngoại vi và thần kinh trung ương.
Bệnh nhân nên được thông báo về những rủi ro liên quan đến fluoroquinolone trước khi bắt đầu điều trị, bao gồm cả tính chất nghiêm trọng và kéo dài của những tác dụng phụ này, đồng thời nên ngừng điều trị và nói chuyện với bác sĩ khi có dấu hiệu hoặc triệu chứng đầu tiên của những phản ứng bất lợi này.
Nên ngừng điều trị bằng fluoroquinolone và cân nhắc điều trị thay thế khi có dấu hiệu của đau gân hoặc viêm hoặc các triệu chứng của bệnh thần kinh như đau, rát, ngứa ran, tê hoặc yếu, để ngăn ngừa sự phát triển của các phản ứng bất lợi có thể không hồi phục.
Không nên kê đơn fluoroquinolon trong những trường hợp sau:
– Nhiễm trùng không nghiêm trọng, có thể tự khỏi như nhiễm trùng cổ họng hoặc các bệnh nhiễm không do vi khuẩn như viêm tuyến tiền liệt (mạn tính).
– Ngăn ngừa bệnh tiêu chảy du lịch hoặc nhiễm trùng đường tiết niệu dưới tái phát (nhiễm trùng nước tiểu không lan ra ngoài bàng quang);
– Nhiễm khuẩn mức độ từ nhẹ đến trung bình (như đợt cấp viêm phế quản mạn tính và bệnh phổi tắc nghẽn mạn tính) trừ khi không có kháng sinh phù hợp thay thế.
– Không kê ciprofloxacin và levofloxacin với viêm bàng quang không phức tạp trừ khi không có kháng sinh phù hợp thay thế.
– Tránh sử dụng fluoroquinolon trên những bệnh nhân đã có tiền sử xuất hiện những phản ứng có hại nghiêm trọng với kháng sinh quinolon (acid nalidixic) và fluoroquinolon.
– Thận trọng khi kê đơn fluoroquinolon cho bệnh nhân trên 60 tuổi, bệnh nhân mắc bệnh thận hoặc ghép tạng do nguy cơ tổn thương gân cao hơn những bệnh nhân khác.
– Tránh sử dụng đồng thời corticosteroid với các kháng sinh fluoroquinolon do làm tăng nguy cơ bị viêm gân và đứt gân gây ra bởi fluoroquinolon.
5.4 Thông tin cho bệnh nhân
Nếu bạn gặp các tác dụng phụ sau đây, hãy ngừng điều trị và liên hệ với bác sĩ ngay lập tức:
– Đau gân hoặc sưng tấy, đặc biệt là ở mắt cá chân hoặc bắp chân. Nếu điều này xảy ra, hãy cho chỗ đau nghỉ ngơi;
– Đau, tê, ngứa ran, sưng tấy hoặc yếu cơ ở các bộ phận khác nhau của cơ thể, thường bắt đầu ở tay hoặc chân, tình trạng này trở nên trầm trọng hơn theo thời gian;
– Mệt mỏi trầm trọng, trầm cảm, trí nhớ kém hoặc khó ngủ nghiêm trọng;
– Thay đổi về thị giác, thính giác, vị giác và khứu giác;
– Sưng ở vai, cánh tay hoặc chân hoặc đau khớp.
– Nếu bạn trên 60 tuổi, có tiền sử bệnh thận hoặc đã được ghép tạng hoặc nếu bạn đang dùng corticosteroid (các loại thuốc như prednisolone hoặc hydrocortisone), bạn sẽ có nguy cơ bị tổn thương gân cao hơn khi dùng fluoroquinolone.
– Bác sĩ sẽ quyết định xem bạn có thể tiếp tục điều trị hay bạn cần một loại kháng sinh khác
– Bạn không nên dùng thuốc fluoroquinolone nếu bạn đã từng gặp tác dụng phụ nghiêm trọng với thuốc fluoroquinolone hoặc thuốc quinolone.
Tài liệu tham khảo
- https://www.gov.uk/drug-safety-update/fluoroquinolone-antibiotics-reminder-of-the-risk-of-disabling-and-potentially-long-lasting-or-irreversible-side-effects
- https://www.ema.europa.eu/en/news/fluoroquinolone-antibiotics-reminder-measures-reduce-risk-long-lasting-disabling-potentially#:~:text=Information%20for%20patients&text=These%20very%20rare%2C%20but%20serious%20side%20effects%20include%20inflamed%20or,and%20altered%20taste%20and%20smell.
- http://canhgiacduoc.org.vn/CanhGiacDuoc/DiemTin/2422/MHRA-nguy-co-phan-ung-co-hai-gay-tan-tat-keo-dai-lien-quan-khang-sinh-fluoroquinolon.htm
HẠN CHẾ ADR TRÊN HỆ TIÊU HÓA VỚI METFORMIN PHÓNG THÍCH KÉO DÀI
6.1 Tổng quan về metformin
Metformin là một thuốc chống đái tháo đường nhóm biguanid, Thuốc không có tác dụng hạ đường huyết ở người không bị đái tháo đường. Ở người đái tháo đường, metformin làm giảm sự tăng đường huyết nhưng không gây tai biến hạ đường huyết. [1]. Metformin là thuốc có bề dày kinh nghiệm sử dụng, được chứng minh về hiệu quả và an toàn; là lựa chọn điều trị bước 1 đái tháo đường tuýp 2 trong tất cả khuyến cáo bao gồm: Hướng dẫn ADA (Hội ĐTĐ Hoa Kỳ), Hướng dẫn IDF (Liên đoàn ĐTĐ Thế giới), Đồng thuận ADA/EASD (Hội N/C ĐTĐ châu Âu) vì hiệu quả hạ đường huyết, không tăng cân, nguy cơ hạ đường huyết quá mức thấp, khả năng dung nạp tốt, không có tác dụng tim mạch bất lợi và chi phí hợp lý [3].
6.1.1 Hiệu quả hạ đường huyết của metformin
Trong một nghiên cứu của nhóm nghiên cứu metformin đa trung tâm Hoa Kỳ (the United States Multicenter Metformin Study Group) đã chỉ định ngẫu nhiên bệnh nhân mắc bệnh tiểu đường loại 2 và béo phì dùng metformin hoặc giả dược [4]. Sau 29 tuần, nồng độ A1C trung bình là 7,1 % ở nhóm metformin so với 8,6 % ở nhóm giả dược; trong nhiều thử nghiệm tiếp theo cũng cho những kết quả tương tự.
6.1.2 Tác dụng có lợi của metformin trên tim mạch
Metformin không có tác dụng tim mạch bất lợi và nó dường như làm giảm các biến cố tim mạch ở một số quần thể nhất định [3]. Metformin có tác dụng hạ lipid, giảm triglyceride huyết thanh và axit béo tự do, giảm LDL và tăng HDL [5].
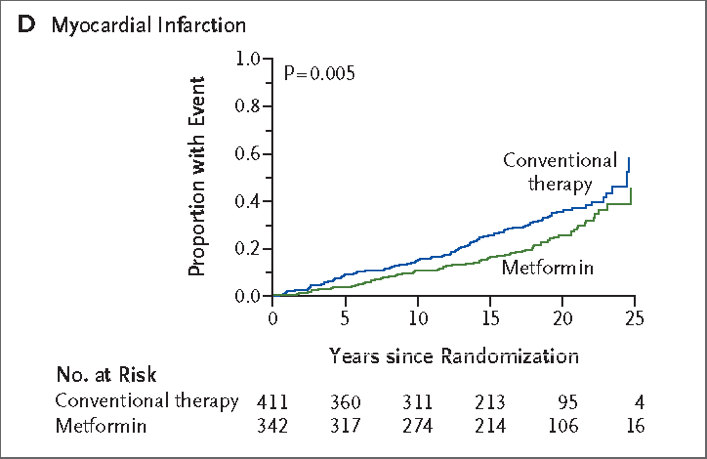
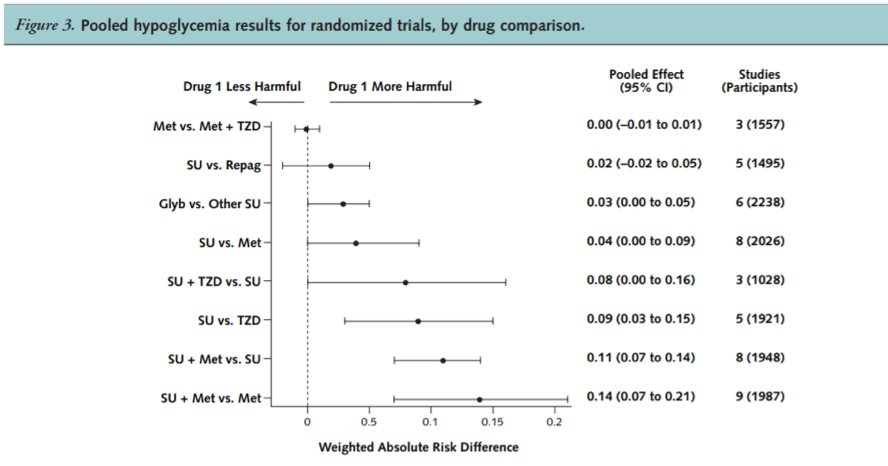
6.1.3 Tỷ lệ hạ đường huyết quá mức liên quan đến metformin thấp
Theo nghiên cứu VADT, hạ đường huyết quá mức là yếu tố gây tử vong cao. Có một số trường hợp báo cáo bị hạ đường huyết quá mức liên quan đến việc dùng metformin, nhưng ước tính tỷ lệ không quá 2% [6], do đó hạ đường huyết quá mức ở liều điều trị của metformin được cho là rất hiếm, nên phác đồ đơn trị và phối hợp điều trị với Metformin được cho là an toàn. Bệnh nhân được khuyên nên dùng metformin cùng với bữa ăn để tránh các khó chịu dạ dày và giảm nguy cơ hạ đường huyết liên quan đến metformin.
6.1.4 Metformin không gây tăng cân
Metformin không gây tăng cân trong quá trình điều trị. Ở những người bị béo phì, metformin thúc đẩy giảm cân ở mức độ vừa phải hoặc ít nhất là ổn định cân nặng [7]. Ví dụ, trong một nghiên cứu lớn, bệnh nhân được điều trị bằng glyburide đã tăng trung bình 1,6 kg, trong khi những người dùng metformin giảm 2,9 kg [8].
6.2 Metformin dạng phóng thích kéo dài (Metformin XR)
Một số ưu điểm của Metformin dạng phóng thích kéo dài (Metformin XR)
– Một nghiên cứu giả dược mù đôi ở Anh được thực hiện trên 240 bệnh nhân đái tháo đường được chọn ngẫu nhiên để dùng metformin XR 1000 mg 1 lần mỗi ngày hoặc giả dược theo tỷ lệ 2:1 trong 12 tuần (bệnh nhân có thể dùng metformin XR 1500 mg trong tuần 12–24 nếu cần). Kết quả thu được metformin XR dùng 1 lần mỗi ngày cải thiện đáng kể việc kiểm soát HbA1C so với việc dùng giả dược ở bệnh nhân đái tháo đường týp 2 mà trước đó đường huyết không được kiểm soát mặc dù đã điều trị bằng chế độ ăn kiêng và tập thể dục (sự khác biệt về HbA1C trong điều trị giữa metformin XR 1000 mg một lần mỗi ngày và giả dược là – 0.7% với p < 0.001). Hiệu quả hạ đường huyết của metformin XR có liên quan đến liều dùng, với hiệu quả tối đa đạt được ở liều 1500 mg một lần mỗi ngày. [9]
– Kiểm soát sự phóng thích ổn định: sau khi uống sự hấp thu metformin chậm lại có ý nghĩa so với dạng phóng thích tức thì với Tmax là 7 giờ (Tmax đối với viên phòng thích tức thì là 2,5 giờ). [2]
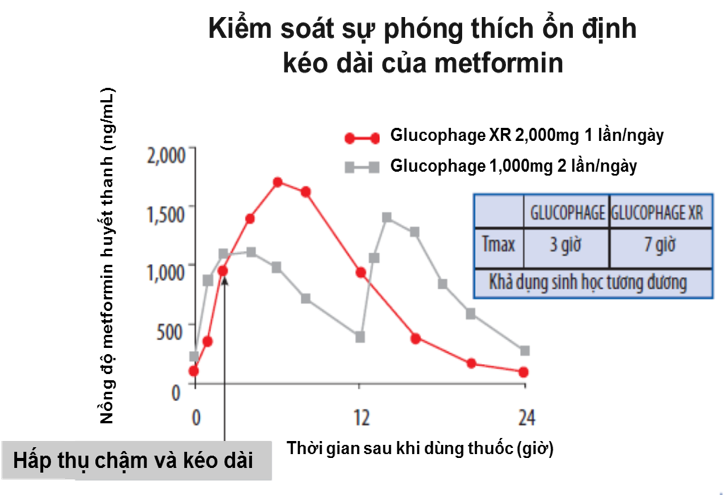
– Cải thiện tác dụng phụ đường tiêu hóa: một nghiên cứu hồi cứu được thực hiện tại Hoa Kỳ được nghiên cứu trên 471 bệnh nhân đái tháo đường tuýp 2 những người đã bắt đầu điều trị ĐTĐ với metformin XR hoặc chuyển từ metformin dạng phóng thích tức thời hoặc thuốc chống đái tháo đường đường uống khác sang metformin XR trong vòng 2 năm. Kết quả cho thấy, việc chuyển từ metformin phóng thích tức thời sang metformin XR đã giúp giảm gần một nửa tỷ lệ tác dụng phụ trên đường tiêu hóa hoặc tác dụng phụ là tiêu chảy. Tương tự như vậy, trong số những bệnh nhân mới điều trị bằng metformin, tỷ lệ mắc các tác dụng phụ trên đường tiêu hóa ở nhóm chỉ dùng metformin phóng thích nhanh gần gấp đôi so với nhóm dùng metformin-XR. [10]
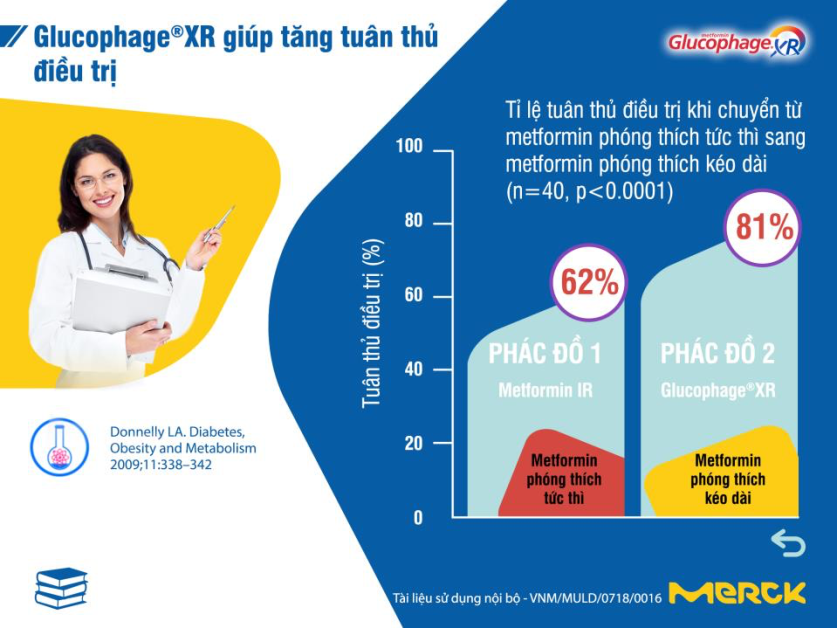
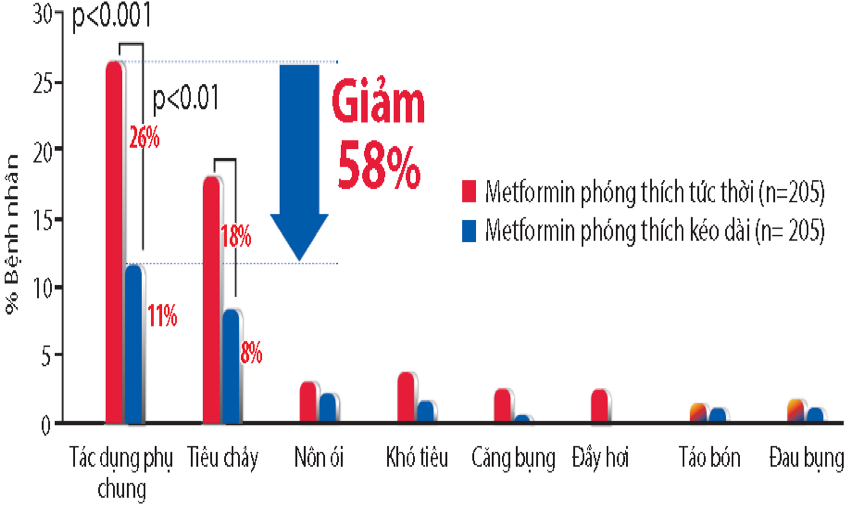 – Tăng tuân thủ điều trị: với metformin XR, bệnh nhân chỉ phải dùng 1 lần/ngày, giúp cải thiện sự thuận tiện cho bệnh nhân dùng liệu pháp metformin để điều trị đái tháo đường. [10] Metformin XR dùng một lần mỗi ngày là một lựa chọn điều trị hiệu quả và dung nạp tốt, hỗ trợ tuân thủ tốt với phác đồ điều trị.
– Tăng tuân thủ điều trị: với metformin XR, bệnh nhân chỉ phải dùng 1 lần/ngày, giúp cải thiện sự thuận tiện cho bệnh nhân dùng liệu pháp metformin để điều trị đái tháo đường. [10] Metformin XR dùng một lần mỗi ngày là một lựa chọn điều trị hiệu quả và dung nạp tốt, hỗ trợ tuân thủ tốt với phác đồ điều trị.
Tài liệu tham khảo
- Dược thư quốc gia Việt Nam (2018).
- Tờ Hướng dẫn sử dụng thuốc Glucophage XR 500 mg
- Maruthur NM, Tseng E, Hutfless S, et al. Diabetes Medications as Monotherapy or Metformin-Based Combination Therapy for Type 2 Diabetes: A Systematic Review and Meta-analysis, Ann Intern Med 2016; 164:740.
- DeFronzo RA, Goodman AM, Efficacy of metformin in patients with non-insulin-dependent diabetes mellitus, The Multicenter Metformin Study Group, N Engl J Med 1995; 333:541.
- Bailey CJ, Turner RC, Metformin, N Engl J Med 1996; 334:574.
- Aldobeaban S, Mzahim B, Ali Alshehri A, Recurrent hypoglycemia secondary to metformin toxicity in the absence of co-ingestions: A case report, J Med Case Rep, 2018;12:223.
- Hemmingsen B, Schroll JB, Wetterslev J, et al, Sulfonylurea versus metformin monotherapy in patients with type 2 diabetes: a Cochrane systematic review and meta-analysis of randomized clinical trials and trial sequential analysis, CMAJ Open 2014; 2:E162.
- Kahn SE, Haffner SM, Heise MA, et al, Glycemic durability of rosiglitazone, metformin, or glyburide monotherapy, N Engl J Med 2006; 355:2427.
- Fujioka, R. L. Brazg, I. Raz, Efficacy, dose–response relationship and safety of once-daily extended-release metformin (Glucophage XR) in type 2 diabetic patients with inadequate glycaemic control despite prior treatment with diet and exercise: results from two double-blind, placebo-controlled studies, Diabetes, Obesity and Metabolism, 7, 2005, 28–39.
- Lawrence Blonde, George E. Dailey, Gastrointestinal tolerability of extended-release metformin tablets compared to immediaterelease metformin tablets: results of a retrospective cohort study, Current medical research and opinion, Vol. 20, No. 4, 2004, 565–572.
[Nguồn: BV YHCT]